This is a SEO version of PAM_350. Click here to view full version
« Previous Page Table of Contents Next Page »50 Panorama Actual del Medicamento
NUEVOS FÁRMACOS
presenta los dos primeros aminoácidos cambiados con respecto a la hirudina natural.
Desirudina fue autorizada en España en 1999 para la prevención de trombosis venosa profunda en pacientes sometidos a cirugía electiva de próte-sis de rodilla y de cadera. En esta indicación, desi-rudina parece producir resultados proflácticos no-tablemente mejores que la heparina convencional y las heparinas de bajo peso molecular, al reducir el riesgo de trombosis venosa profunda en un 50-70% en relación a la heparina no fraccionada, y en un 30% frente a enoxaparina. La diferencia es aun más marcada en la prevención de las trombosis proximales (40-90%). Sin embargo, no existe antí-doto para la desirudina y la sobredosis de desiru-dina puede causar graves complicaciones hemorrá-gicas, lo que oblliga a un cuidadoso manejo. Otro análogo de la hirudina, lepirudina , fue autorizada para su uso en pacientes con trombocitopenia in-ducida por heparina .
En 2004 se autorizó en la Unión Europea ximela-gatrán (Exanta ® ), un inhibidor directo, competitivo y reversible de la trombina, el enzima que convierte el fbrinógeno en fbrina en la cascada de coagu-lación; por lo tanto, la inhibición de la trombina previene el desarrollo de trombos. Sin embargo, el medicamento fue retirado en 2006, debido a la aparición de cuadros graves de hepatotoxicidad. Posteriormente, en 2008, se comercializó dabiga-trán (Pradaxa ® ), estrechamente relacionado con el anterior, un peptidomimético que emula parte de la estructura del fbrinógeno y que se une específ-camente en la zona catalítica de la trombina, inhi-biendo temporalmente su actividad. Fue autorizada para la prevención primaria de tromboembolismos venosos en adultos sometidos a cirugía programada de reemplazo total de cadera o de rodilla.
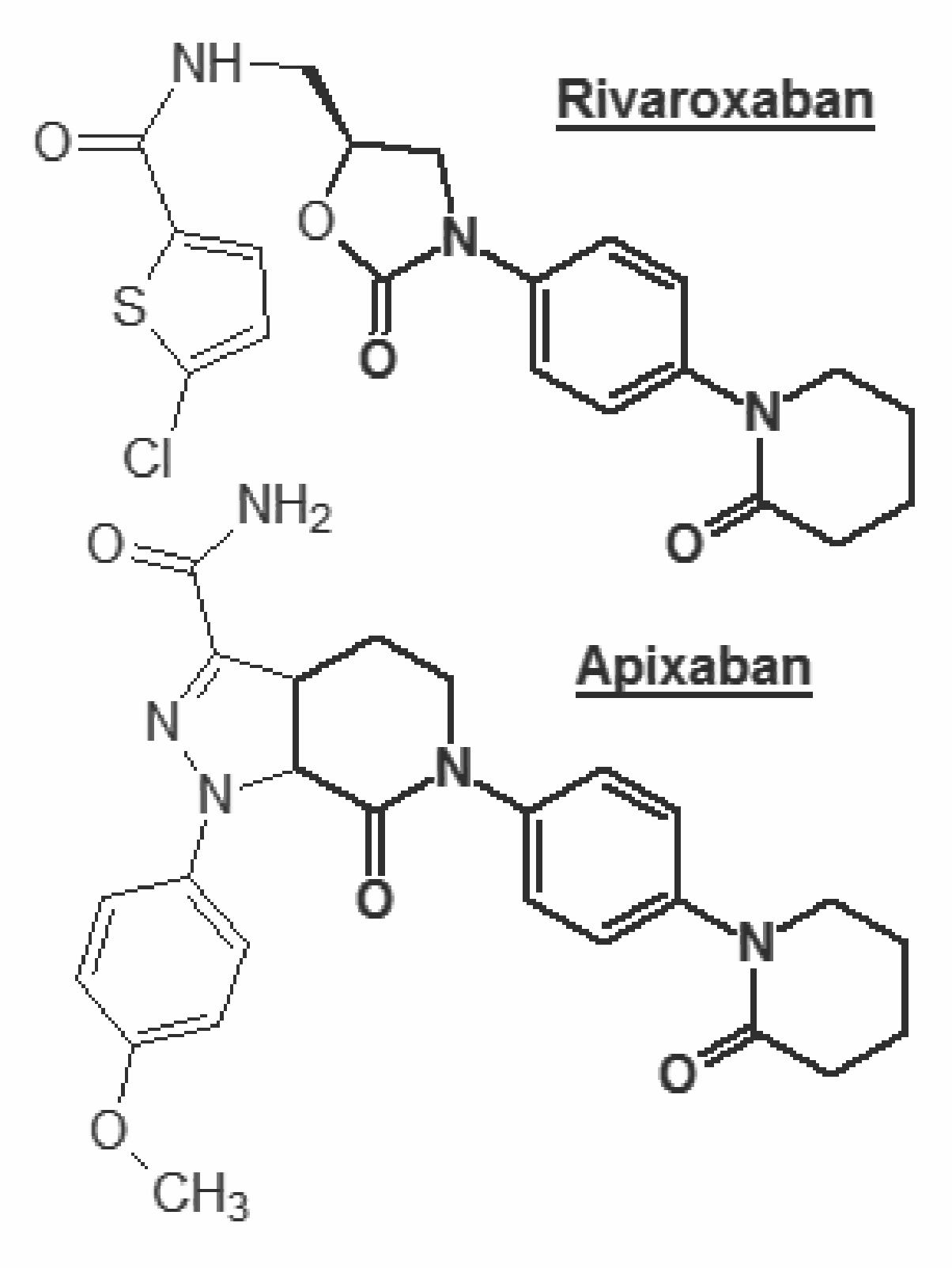
Poco después del dabigatrán fue comercializado el rivaroxabán (Xarelto ® ), que actúa inhibiendo de forma directa y selectiva el Factor Xa, el cual ocupa una posición crítica en el proceso de coagulación, convirtiendo la protombina (Factor II) en trombina (Factor IIa). Una molécula de Factor Xa cataliza la formación de aproximadamente 1.000 moléculas de trombina. De esta manera, la inhibición del Fac-tor Xa es susceptible de prevenir de forma efcaz los trombos arteriales ricos en plaquetas y los trombos venosos ricos en fbrina. La inhibición selectiva del Factor Xa por rivaroxabán puede inhibir la formación de trombina, pero permitiendo al mismo tiempo que la trombina previamente formada efectúe sus fun-ciones normales en la hemostasia. La inhibición de rivaroxabán sobre el Factor Xa tiene carácter com-petitivo y reversible, siendo unas 10.000 veces más selectivo frente al Factor Xa que frente a otros enzi-mas de tipo serina proteasa humanos.
ACCIÓN Y MECANISMO
Apixabán es un agante antitrombótico autorizado para la prevención del tromboembolismo venoso en pacientes adultos sometidos a cirugía electiva de reem-plazo de cadera o rodilla. Actúa inhibiendo de forma directa y selectiva el Factor Xa, que ocupa una posición crítica en el proceso de coagulación, convirtiendo la protombina (Factor II) en trombina (Factor IIa). Una molécula de Factor Xa cataliza la formación de aproximadamente 1.000 moléculas de trombina. De esta manera, la inhibición del Factor Xa es susceptible de prevenir de forma efcaz los trombos arteriales ricos en plaquetas y los trombos venosos ricos en fbrina. La inhibición selectiva del Factor Xa por apixabán puede inhibir la formación de trombina, pero permitiendo al mismo tiempo que la trombina previamente formada efectúe sus funciones normales en la hemostasia.
ASPECTOS MOLECULARES
Apixabán está estructuralmente relacionado con el rivaroxabán. La estructura emula un pequeño péptido que es capaz de actuar como falso sustrato
This is a SEO version of PAM_350. Click here to view full version
« Previous Page Table of Contents Next Page »